Exufiber i praksis
Tilstanden til omkringliggende hud ble bedre og diabetiske fotsår minket i størrelse i en studie med 21 pasienter som ble behandlet med Exufiber®.
Åpen, ikke-sammenlignbar, multisenter postklinisk studie av ytelsen og sikkerheten til geldannende fiberbandasjer på diabetiske fotsår
Chadwick, P., McCardle, J. Journal of Wound Care 2016; 25(4):290-300.
- Fotsår hos diabetiske pasienter er vanskelig å behandle.
- Pasienter med dårlig håndtert diabetes har økt risiko for fotsår og fotamputasjon.
- Valg av riktig bandasje er viktig i behandlingen av diabetiske fotsår.
- Diabetiske fotsår er forbundet med medisinske utgifter, i tillegg til private, sosiale og økonomiske kostnader.
- I likhet med andre kroniske sår kan diabetiske fotsår produsere store mengder sårvæske, og det skaper risiko for maserasjon for omkringliggende hud.
Mål
Evaluere ytelsen og sikkerheten til Exufiber geldannende fiberbandasje i behandlingen av diabetiske fotsår.
Metoder
- Dette var en åpen, ikke-sammenlignbar multisenter undersøkelse.
- Studien omfattet både innlagte og polikliniske pasienter.
Primærmål for studien:
- Evaluere ytelsen og sikkerheten til Exufiber ved tiltenkt bruk på diabetiske fotsår.
- I tråd med dette målet ble en rekke evalueringsparametere målt for å overvåke tilstanden til omkringliggende hud (endringer i forhold til baseline-vurderinger): maserasjon; rødhet/irritasjon; utslett/eksem; blemmer; dermatitt; skader i huden; skade på sårkanten; produktforringelse på huden.
Sekundærmål for studien:
- Evaluering av bandasjerelatert smerte (målt med en 100 mm visuell analog skala (VAS)).
- Sårtilstand (målt med endringer i sårstørrelse og helingsfase).
- Legens/pasientens meninger om testproduktet.
- Teknisk ytelse av testproduktet (målt med mengden bandasjerester etter fjerning samt håndtering av sårvæske).
- Pasienter med flere sår deltok i undersøkelsen, men kun ett sår per pasient ble undersøkt.
- Hver pasient ble behandlet i henhold til lokal klinisk prosedyre, og alle bandasjer ble applisert i henhold til produsentens instruksjoner.
- Pasientene deltok i undersøkelsen frem til fullført sårheling eller hvis behandlet sår ble tørt (og testproduktet ikke lenger kunne brukes) eller i 12 uker, avhengig av hva som inntraff først.
- Pasientene ble vurdert ved baseline og på nytt 1, 2, 4, 6, 8 og 12 uker etter behandling.
- Bandasjeskiftene ble utført i henhold til lokal klinisk prosedyre (vanligvis 3 ganger per uke) når bandasjen var mettet og avhengig av sårets tilstand og plassering, men bandasjeskift mellom kontroller var tillatt.
- Ved hver kontroll ble følgende variabler vurdert:
- Sårstørrelse, volum (med PictZar-programmet) og dybde på sårets dypeste punkt (med Q-tips); målingene ble utført hver fjerde uke og en ekstra måling ble foretatt i uke 6)
- Utseendet på sårsengen
- Tilstanden til omkringliggende hud
- Teknisk ytelse
- Mengden og typen sårvæske
- Behov for debridering
- Bivirkninger / ugunstig effekt av utstyr (ADE)
- Smerte (før fjerning av sekundærbandasje; før fjerning av testprodukt; ved fjerning av testprodukt; etter fjerning av testprodukt). Enkelte pasienter deltok ikke i smertevurderingen pga. nevropati
- Kliniske tegn på infeksjon
Resultater
- 21 pasienter fra to helseinstitusjoner deltok i undersøkelsen.
- Alle pasientene (som var egnet for behandling med testproduktet) var europeiske menn med et aktivt diabetisk fotsår, og pasientenes snittalder var 59,9 år.
Tilstanden til omkringliggende hud
- Antallet pasienter med frisk/intakt omkringliggende hud økte fra 6 pasienter (28,6 %) ved baseline til 14 pasienter (66,7 %) ved siste kontroll.
- Prosentandelen med pasienter med et gitt tegn på dårlig tilstand for omkringliggende hud gikk ned eller holdt seg på null for de fleste tegnene, fra baseline til siste kontroll.
- Det var ingen forekomster av produktforringelse på huden.
Sårvæske
- Det var en jevn nedgang i mengden sårvæske gjennom hele studieperioden; prosentandelen med pasienter uten sårvæske økte fra 0 % ved baseline til 33,3 % i uke 12.
- Sårvæske var for det meste serøs (klar og blank) i studieperioden.
Smerte
- Smertenivåene var svært lave i studieperioden (enkelte pasienter kunne ikke delta i smertevurderingen pga. nevropati eller fullført sårheling).
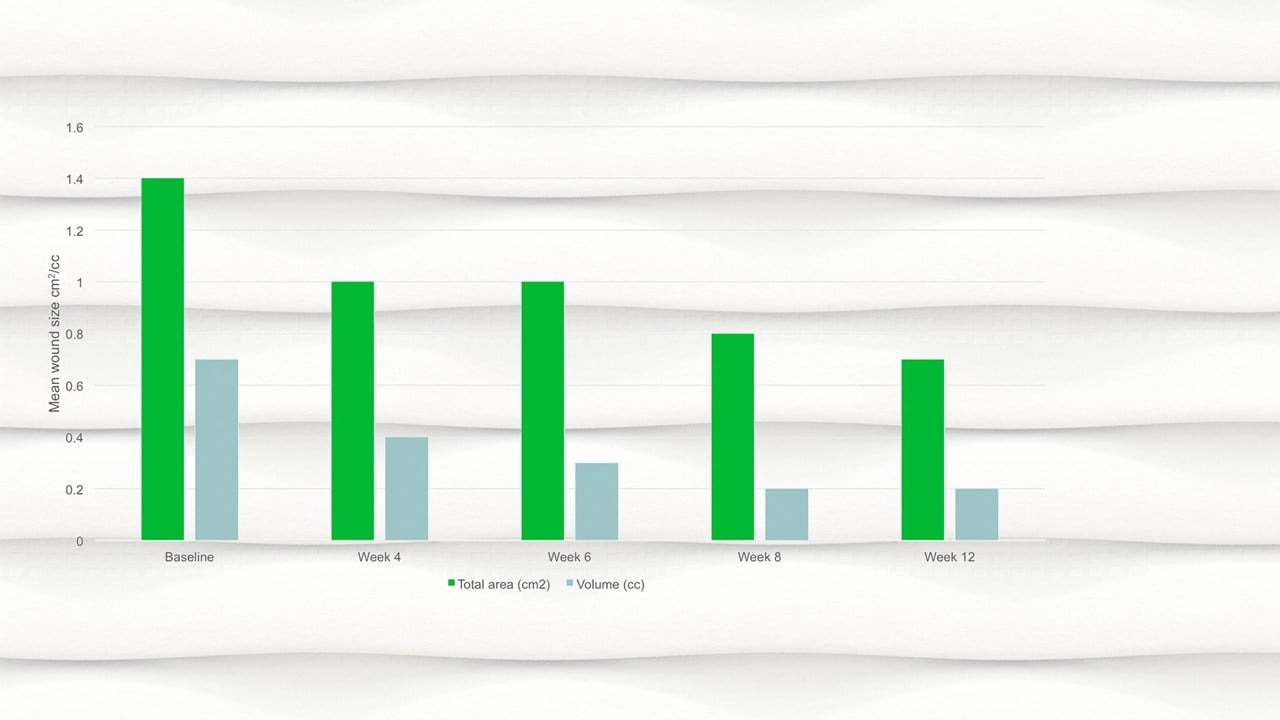
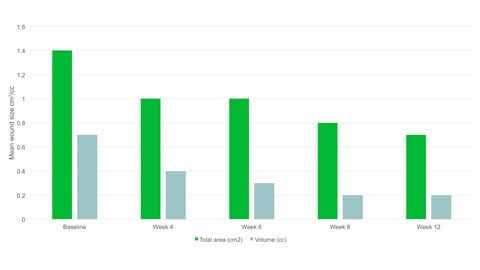
Sårtilstand
- Innen uke 12 var gjennomsnittlig sårområde halvert sammenlignet med baseline, med et snittområde på 0,7 cm2.
- Det var en signifikant reduksjon av sårområde (p=0,094) og sårvolum (p=0,0056) fra baseline til siste kontroll.
- Det var en gradvis økning i gjennomsnittlig prosentandel av epitelisering av vev og en liten nedgang i gjennomsnittlig prosentandel av granulasjonsvev gjennom hele studieperioden; prosentandelen av ikke-levedyktig vev forble lav gjennom studien.
- Antallet helede sår økte fra 1 (4,8 %) i uke 1 til 5 (23,8 %) i uke 12.
Kliniske tegn på infeksjon
Nivået på kliniske tegn på infeksjon var lavt gjennom hele studieperioden.
Undersøkers/sykepleiers evaluering
Den evaluerte bandasjen skåret høyt på at den var enkel å applisere, enkel å fjerne, den heftet ikke til sårsengen og frisk hud forble intakt ved fjerning, den var fleksibel, formbar, absorberte sårvæske, holdt på tykk sårvæske og blod, og på den totale opplevelsen.
Pasientens evaluering
Den evaluerte bandasjen skåret høyt på manglende engstelse ved bandasjeskift, god bevegelsesfrihet, at bandasjen holdt seg på plass ved bruk, mangelen på stikking eller svie ved bruk av bandasjen og komfort ved bruk.
Det ble ikke rapportert om bivirkninger / ugunstig effekt av utstyr (ADE) i løpet av studien som ble vurdert å ha sammenheng med det undersøkte produktet.
Konklusjoner
- Resultatet av studien viser at den undersøkte sårbandasjen minimerer skade på omkringliggende hud og bandasjerelatert smerte.
- Selv om de fleste sårene ikke var helet mot slutten av studieperioden, så ble det registrert forbedringer i vevstype og en signifikant reduksjon i sårområde og sårvolum.
- Bandasjens tekniske ytelse ble vist ved at den klarte å absorbere og holde på sårvæske.
- Produktsikkerhet ble vist med en økning i antallet pasienter med frisk/intakt omkringliggende hud og mangelen på produktrelaterte bivirkninger / ugunstig effekt av utstyr.





