Exufiber i praksis
Hudens tilstand omkring såret blev forbedret, og diabetiske fodsår blev reduceret i størrelse i et forsøg med 21 patienter, der blev behandlet med Exufiber®.
Et åbent, ikke-sammenlignende, postklinisk multicenterforsøg af resultater og sikkerhed ved en gelerende fiberbandage på diabetiske fodsår
Chadwick, P., McCardle, J. Journal of Wound Care 2016; 25(4):290-300.
- Det er vanskeligt at behandle fodsår hos diabetiske patienter.
- Patienter med dårligt reguleret diabetes er i risiko for at få fodsår og amputation af foden.
- Valget af bandage er ét vigtigt aspekt ved behandling af diabetiske fodsår.
- Diabetiske fodsår er forbundet med medicinske udgifter såvel som personlig, sociale og økonomiske omkostninger.
- I lighed med andre kroniske sår producerer diabetiske fodsår store mængder ekssudat. Såromgivelserne er derfor i risiko for maceration.
Mål
At vurdere resultaterne og sikkerheden ved Exufiber, en gelerende fiberbandage, til behandling af diabetiske fodsår.
Metoder
- Dette var en åben, ikke-sammenlignende multicenterundersøgelse.
- Både indlagte patienter og ambulante patienter var egnede.
Det primære forsøgsformål:
- At vurdere resultaterne og sikkerheden ved Exufiber, når det blev brugt efter hensigten på diabetiske fodsår.
- I overensstemmelse med dette formål blev et antal parametre målt med henblik på at monitorere såromgivelserne (vurdering af ændringer i sammenligning med målingerne ved baseline): maceration; rødme/irritation; udslæt/eksem; blæredannelse; dermatitis; hudstripping; traume i sårkanterne; produktnedbrydning på huden.
Sekundære forsøgsformål:
- Vurdering af bandagerelaterede smerter (målt ved hjælp af en 100 mm visuel analog skala (VAS-skala)).
- Sårstatus (målt ved ændringer i sårstørrelse og helingsfase).
- Lægens/patientens mening om testproduktet.
- Testproduktets tekniske ydeevne (målt ved tilstedeværelse af bandagerester efter aftagning af bandagen og håndtering af ekssudat fra såret).
- Patienter med mere end et sår var egnede til inklusion i undersøgelsen, men kun et sår pr. patient blev inkluderet i undersøgelsen.
- Hver enkelt patient blev behandlet i henhold til lokal klinisk rutine, og alle bandager blev appliceret i henhold til producentens instruktioner.
- Patienterne deltog i undersøgelsen indtil komplet sårheling, eller til det behandlede sår blev tørt (hvorved testproduktet ikke længere var anvendeligt) eller i 12 uger, alt efter hvad der skete først.
- Patienterne blev vurderet ved baseline og igen i uge 1, 2, 4, 6, 8 og 12 efter behandlingen.
- Bandageskift blev foretaget i henhold til lokal klinisk rutine (normalt 3 gange om ugen), når bandagen var gennemvædet og afhængigt af sårets status og placering. Bandageskift mellem besøgene var tilladt.
- Ved hvert vurderingsbesøg blev følgende variable vurderet:
- Sårstørrelse, volumen (ved hjælp af Pictzar-programmet) og dybden af det dybeste punkt i såret (ved hjælp af en vatpind). Målingerne foretaget hver 4. uge med en ekstra måling i uge 6.
- Sårbundens udseende
- Såromgivelsernes tilstand
- Tekknisk ydeevne
- Mængde og type af ekssudat
- Behov for debridering
- Utilsigtede hændelser (AE'er)/utilsigtede hændelser med udstyr (ADE'er)
- Smerter (før aftagning af den sekundære bandage; før aftagning af testproduktet; under aftagning af testproduktet; efter aftagning af testproduktet). Nogle patienter var uegnede til inklusion i smertevurderingen på grund af neuropati
- Kliniske tegn på infektion
Resultater
- 21 patienter fra to forsøgscentre var inkluderet i undersøgelsen.
- Alle de rekrutterede patienter (egnet til behandling med testproduktet) var kaukasiske mænd med et aktivt fodsår. Den gennemsnitlige alder på patienterne var 59,9 år.
Såromgivelsernes tilstand
- Antallet af patienter med sund/intakt hud rundt om såret steg fra 6 patienter (28,6%) ved baseline til 14 patienter (66,7%) ved det afsluttende besøg.
- Procentdelen af patienter med et givet tegn på dårlig status for såromgivelserne faldt eller forblev på nul for størstedelen af tegnene fra baseline til det afsluttende besøg.
- Der var ingen forekomst af produktnedbrydning på huden.
Ekssudat fra såret
- Der var et støt fald i mængden af ekssudat gennem hele forsøgsperioden. Procentdelen af patienter uden ekssudat steg fra 0% ved baseline til 33,3% i uge 12.
- Ekssudatet var primært serøst gennem hele forsøgsperioden.
Smerter
- Smerteniveauet var meget lavt i hele forsøgsperioden (nogle patienter var ikke egnede til inklusion i smertevurderingen på grund af neuropati eller afslutning af sårheling).
Sårstatus
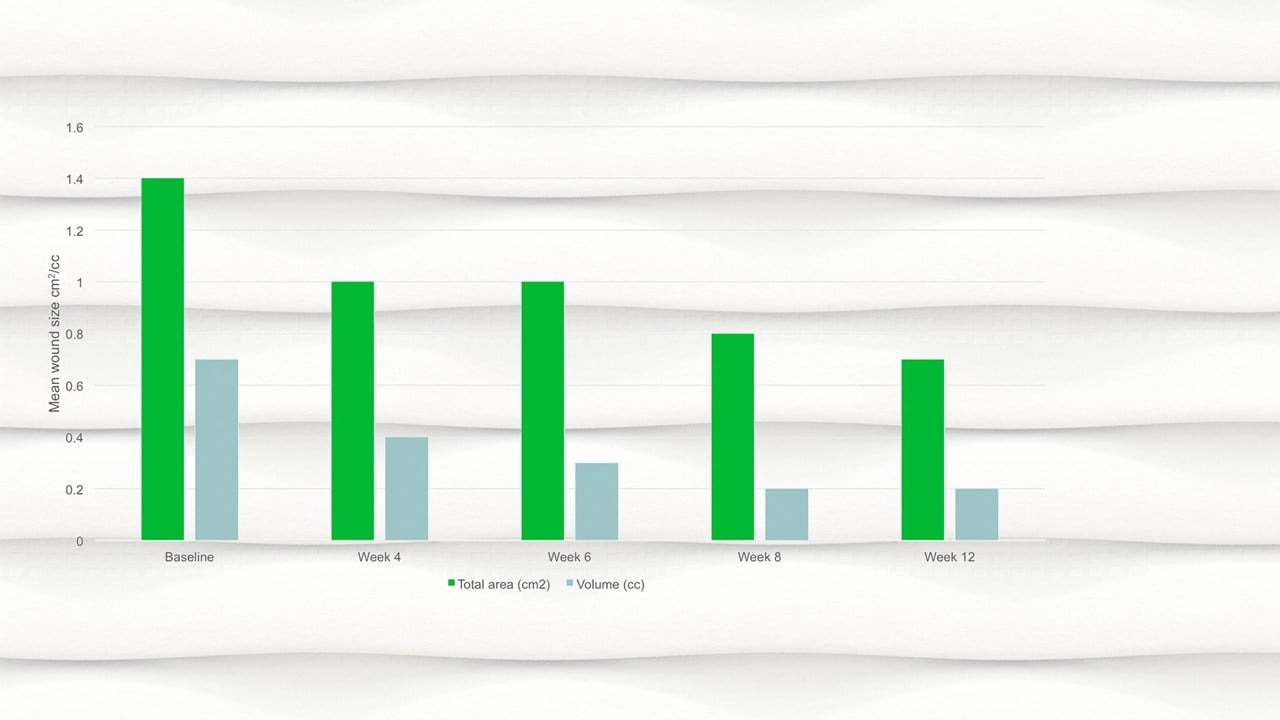
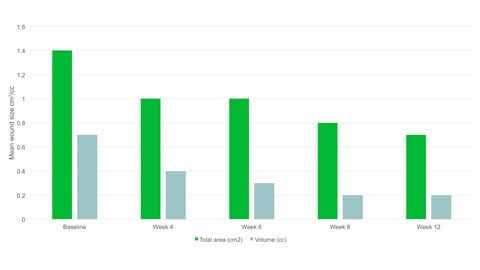
- I uge 12 var det gennemsnitlige omfang af såret halveret sammenlignet med baseline med et gennemsnitligt areal på 0,7cm2.
- Der var en signifikant reduktion i sårareal, p=0,094, og sårvolumen, p=0,0056, fra baseline til det afsluttende besøg.
- Der var en gradvis stigning i den gennemsnitlige procentdel af epithelialiseringsvæv og et lille fald i den gennemsnitlige procentdel af granulationsvæv gennem hele forsøget. Procentdelen af ikke-levedygtigt væv forblev lavt gennem hele forsøget.
- Antallet af helede sår steg fra 1 (4,8%) i uge 1 til 5 (23,8%) i uge 12.
Kliniske tegn på infektion
Der var et lavt niveau af kliniske tegn på infektion i hele forsøgsperioden.
Investigators/sygeplejerskes vurdering
Bandagen, der skulle vurderes, blev bedømt højt med hensyn til nem at applicere, nem at aftage, klæbe ikke på sårbunden og sund, intakt hud ved aftagning, fleksibilitet, formbarhed, evne til at absorbere ekssudat, evne til at binde dødt væv og den samlede oplevelse.
Patientens vurdering
Bandagen, der skulle vurderes, blev bedømt højt med hensyn til ingen frygt i forbindelse med bandageskift, nem bevægelighed, når man går med bandagen, bandagens evne til at blive siddende under brug, ingen stikkende eller brændende fornemmelse ved brug og behagelighed ved brug.
Der var ingen rapporterede AE'er/ADE'er i løbet af forsøget, som blev bedømt til at være relaterede til forsøgsproduktet.
Konklusioner
- Resultaterne fra dette forsøg har vist forsøgsbandagens evne til at mindske skader på såromgivelserne samt bandagerelaterede smerter.
- Selv om de fleste sår stadig ikke var helede ved afslutningen af forsøgsperioden, blev der noteret forbedringer i form af vævstype og en signifikant reduktion af sårets omfang og volumen.
- Bandagens tekniske ydeevne blev vist ved en evne til at absorbere og binde ekssudat.
- Produktets sikkerhed blev vist ved en stigning i antallet af patienter med sund/intakt hud rundt om såret og manglen på identificerede, produktrelaterede AE'er/ADE'er.









