Exufiber in de praktijk
De conditie van de huid rond de wond verbeterde en diabetische voetulcera namen in omvang af in een onderzoek onder 21 patiënten die met Exufiber® werden behandeld.
Open, non-comparative, multi-centre post clinical study of the performance and safety of a gelling fibre wound dressing on diabetic foot ulcers
Chadwick, P., McCardle, J. Journal of Wound Care 2016; 25(4):290-300,
- Voetulceratie bij diabetespatiënten is moeilijk te behandelen.
- Patiënten bij wie de diabetes slecht onder controle is, lopen een verhoogd risico op voetulceratie en -amputatie.
- De verbandkeuze is een belangrijk aspect van de behandeling van diabetisch voetulcus (diabetic foot ulcus, DFU).
- DFU's gaan niet alleen gepaard met medische kosten, maar hebben ook een persoonlijke, maatschappelijke en economische kost.
- Net als andere chronische wonden kunnen DFU's veel exsudaat produceren. Als gevolg daarvan bestaat het risico van maceratie van de huid rondom de wond.
Doelstellingen
De prestaties en veiligheid beoordelen van Exufiber®, een gelvormend vezelverband, bij de behandeling van DFU's.
Methodes
- Dit was een open, niet-vergelijkend, multicentrisch onderzoek.
- Zowel poliklinische als intramurale patiënten kwamen in aanmerking voor deelname.
Primaire onderzoeksobjectieven:
- De prestaties en veiligheid van Exufiber® beoordelen bij het beoogde gebruik voor de behandeling van DFU's.
- In overeenstemming met deze doelstelling werden een aantal beoordelingsparameters gemeten om de conditie van de huid rond de wond te monitoren (beoordeeld in termen van veranderingen ten opzichte van de baseline-beoordelingen): maceratie; roodheid/irritatie; uitslag/eczeem; blaarvorming; dermatitis; loslatende huid; trauma aan de wondranden; productdegradatie op de huid.
Secundaire onderzoeksobjectieven:
- Het beoordelen van aan het verband gerelateerde pijn (gemeten met behulp van een 100mm visueel analoge schaal (VAS).
- Wondstatus (gemeten aan de hand van veranderingen in de wondgrootte en genezingsfase).
- Mening van arts/patiënt over het testproduct.
- Technische prestaties van het testproduct (gemeten aan de hand van de aanwezigheid van verbandresten na verwijdering en de behandeling van wondexsudaat).
- Patiënten met meer dan één ulcus kwamen in aanmerking voor deelname aan het onderzoek, hoewel slechts één ulcus per patiënt werd opgenomen in het onderzoek.
- Iedere patiënt werd behandeld volgens de lokale klinische routine en alle verbanden werden aangebracht conform de instructies van de fabrikant.
- Patiënten namen deel aan het onderzoek tot de wond volledig genezen was of de behandelde wond droog werd (waarna het testproduct niet langer van toepassing was) of gedurende 12 weken, wat zich het eerste voordeed.
- Patiënten werden beoordeeld op baseline en opnieuw in week 1, 2, 4, 6, 8 en 12 na behandeling.
- Verbandwissels werden uitgevoerd volgens de lokale klinische routine de (gewoonlijk 3 keer per week) wanneer het verband doorweekt was en afhankelijk van de status en locatie van de wond; verbandwissels tussen de bezoeken waren toegestaan.
- Bij elk beoordelingsbezoek werden de volgende variabelen geëvalueerd:
- Wondgrootte, volume (met behulp van het Pictzar-programma) en de diepte op het diepste punt van de wond (met behulp van een wattenstaafje); de metingen vonden om de vier weken plaats, met een extra meting in week 6)
- Uiterlijk van het ulcusbed
- Conditie van de huid rond de wond
- Technische prestaties
- Hoeveelheid en type wondexsudaat
- Behoefte aan débridement
- Ongewenste voorvallen (adverse events, AE's)/ongewenste voorvallen verband houdend met het hulpmiddel (ADE's)
- Pijn (voor het verwijderen van het secundaire verband; voor het verwijderen van het testproduct; tijdens het verwijderen van het testproduct; na het verwijderen van het testproduct). Sommige patiënten kwamen niet in aanmerking voor deelname aan de pijnbeoordeling vanwege neuropathie
- Klinische tekenen van infectie
Resultaten
- 21 patiënten uit twee centra werden toegelaten tot het onderzoek.
- Alle toegelaten patiënten (die in aanmerking kwamen voor behandeling met het testproduct) waren blanke mannen met een actieve DFU; de gemiddelde leeftijd van de patiënten was 59,9 jaar.
Conditie van de huid rond de wond
- Het aantal patiënten met gezonde/intacte huid rond de wond nam toe van 6 patiënten (28,6%) op baseline tot 14 patiënten (66,7%) bij het eindbezoek.
- Het percentage patiënten met een bepaald teken van een slechte huidstatus rond de wond nam af of bleef nul bij het merendeel van de tekenen, van baseline tot het eindbezoek.
- Er waren geen gevallen van productdegradatie op de huid.
Wondexsudaat
- Er was een gestage afname van het wondexsudaatvolume gedurende de onderzoeksperiode; het percentage patiënten zonder wondexsudaat steeg van 0% op baseline naar 33,3% in week 12.
- Gedurende de hele onderzoeksperiode was het wondexsudaat voornamelijk sereus.
Pijn
- De pijnniveaus waren zeer laag gedurende de gehele onderzoeksperiode (sommige patiënten kwam niet in aanmerking voor deelname aan de pijnbeoordeling vanwege neuropathie of omdat het ulcus volledig genezen was).
Wondstatus
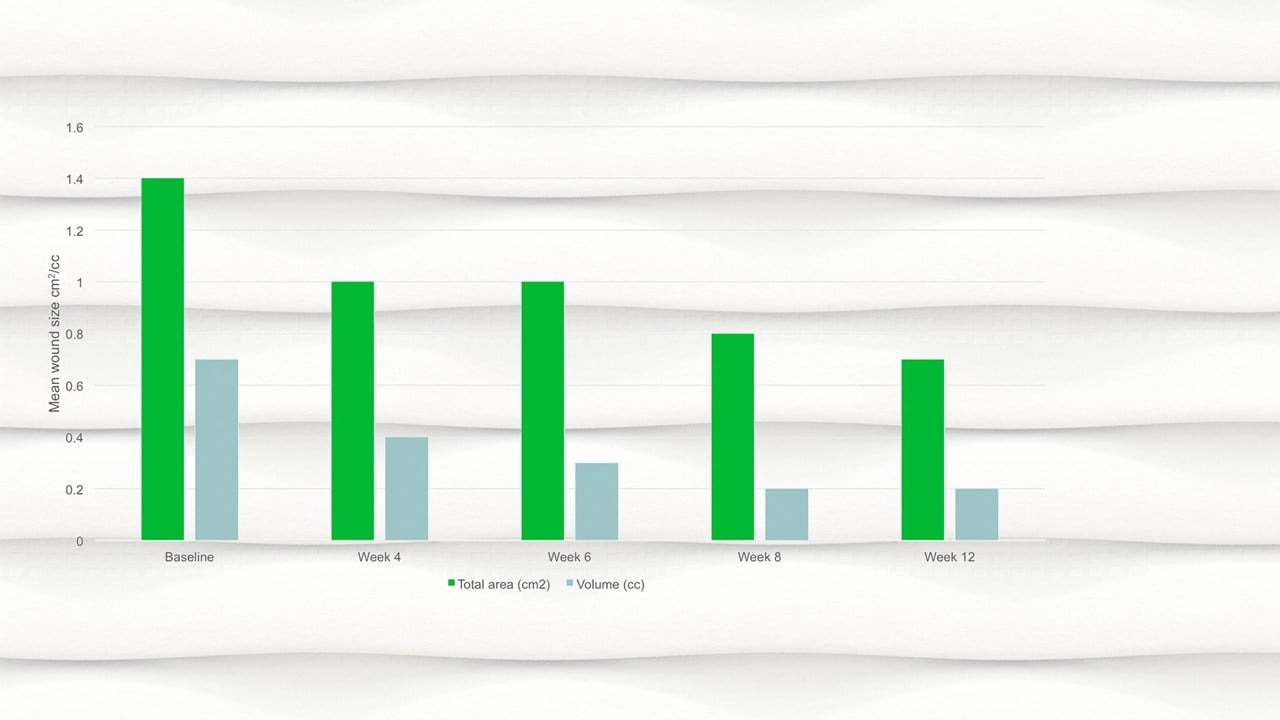
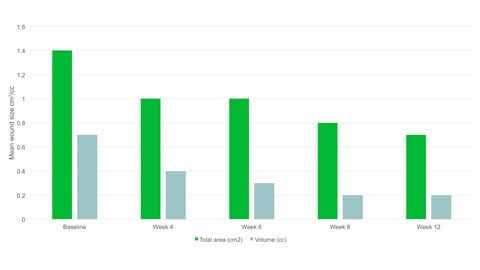
- Tegen week 12 was het gemiddelde wondgebied gehalveerd ten opzichte van baseline, met een gemiddeld gebied van 0,7cm².
- Er was sprake van een significante afname van het wondgebied, p=,094 en het wondvolume, p=,0056 van baseline tot het eindbezoek.
- Verder werden gedurende het onderzoek een geleidelijke toename van het gemiddelde percentage epithelialisatieweefsel en een kleine afname van het gemiddelde percentage granulatieweefsel waargenomen; het percentage niet-levensvatbaar weefsel bleef laag tijdens het onderzoek.
- Het aantal genezen wonden steeg van 1 (4,8%) in week 1 naar 5 (23,8%) in week 12.
Klinische tekenen van infectie
Het aantal klinische tekenen van infectie bleef gering gedurende de hele onderzoeksperiode.
Beoordeling door onderzoeker/verpleegkundige
Het beoordeelde verband werd hoog gewaardeerd wat betreft het gemak van aanbrengen en verwijderen, het feit dat het bij verwijdering niet aan het wondbed en de gezonde intacte huid kleefde, de flexibiliteit, de soepelheid, het absorptievermogen op vlak van exsudaat, het vermogen om dood weefsel en bloed vast te houden en de algehele beleving.
Beoordeling door de patiënt
Het beoordeelde verband werd hoog gewaardeerd omdat men geen van angst had tijdens verbandwissels en vanwege de bewegingsvrijheid tijdens het dragen van het verband, het feit dat het verband tijdens het dragen goed op zijn plaats bleef en niet voor een prikkend of brandend gevoel zorgde, en het draagcomfort.
In het verloop van het onderzoek werden geen AE's/ADE's gemeld die gerelateerd werden aan het onderzoeksproduct.
Conclusies
- De resultaten van deze studie hebben aangetoond, dat het onderzoeksverband het vermogen heeft om schade aan de huid rond de wond en de pijn in samenhang met het verband te minimaliseren.
- Hoewel de meeste wonden aan het einde van het onderzoek nog niet genezen waren, werden verbeteringen in termen van weefseltype en een significante afname van het wondgebied en -volume waargenomen.
- De technische prestaties van het verband werden aangetoond aan de hand van het vermogen om exsudaat te absorberen en vast te houden.
- De productveiligheid werd aangetoond aan de hand van een toename van het aantal patiënten met gezonde/intacte huid rond de wond en het ontbreken van productgerelateerde AE's/ADE's.








